第1回Quimica模試【2017年6月25日】
Quiz-summary
0 of 25 questions completed
Questions:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
Information
今から出題される問題に答えよ。(制限時間60分)
You have already completed the quiz before. Hence you can not start it again.
問題を読込中…
You must sign in or sign up to start the quiz.
You have to finish following quiz, to start this quiz:
テスト結果
0問/25問中正解です。
所要時間:
制限時間になりました。
あなたの正解率は0点/0点中0です。
Categories
- Not categorized 0%
-
あなたの偏差値は80です。
-
あなたの偏差値は75です。
-
あなたの偏差値は70です。
-
あなたの偏差値は65です。
-
あなたの偏差値は60です。
-
あなたの偏差値は55です。
-
あなたの偏差値は50です。
-
あなたの偏差値は45です。
-
あなたの偏差値は40です。
-
あなたの偏差値は35です。
-
あなたの偏差値は30です。
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
- Answered
- Review
-
1問/25問
1. 問題
1.次のa~eに当てはまるものを,解答群のうちから一つずつ選べ。
a 電子の総数がCH₄と同じ分子
正解
不正解
-
2問/25問
2. 問題
b 結合に用いられている電子の総数が,6個である分子
正解
不正解
-
3問/25問
3. 問題
c 構造式で表したときに,価標の数が最も多い分子
正解
不正解
-
4問/25問
4. 問題
d 三重結合をもつ分子
正解
不正解
-
5問/25問
5. 問題
e 互いに同素体でないもの
正解
不正解
-
6問/25問
6. 問題
正解
不正解
-
7問/25問
7. 問題
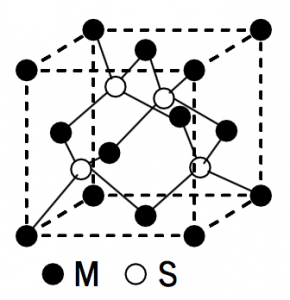
(2) この硫化物に含まれる金属の含有量は67.1%であった。この金属の原子量を有効数字2桁で求めよ。
正解
不正解
-
8問/25問
8. 問題
(3) 図の金属原子と硫黄原子を炭素原子で置き換えるとダイヤモンドの結晶構造の単位格子となる。ダイヤモンドの単位格子に含まれる炭素原子の数はいくらか。
正解
不正解
-
9問/25問
9. 問題
(4) ダイヤモンドでは各炭素原子は一辺の長さ 2.53×10⁻¹⁰ m の正四面体形をつくる 4 個の炭素原子に囲まれている。ダイヤモンドの単位格子の一辺の長さを有効数字3桁で求めよ。√2=1.414
- (3.56)×10⁻¹⁰ m
正解
不正解
-
10問/25問
10. 問題
(5) ダイヤモンドの密度は何 g/cm³ か。有効数字3桁で求めよ。
- (3.52)g/cm³
正解
不正解
-
11問/25問
11. 問題
3.容積 2.0 L の容器 A と容積 3.0 L の容器 B を,体積の無視できる管でつなぎ,0.25 mol の窒素を入れた。この後, 容器 A を 27°C,容器 B を 127°C に保つと,容器内の圧力は何 Pa になるか。有効数字2桁で求めよ。
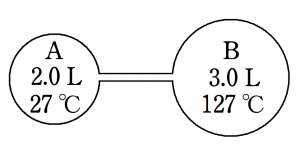
- (1.5)×10⁵ Pa
正解
不正解
-
12問/25問
12. 問題
4.物質が水に溶けるときに出入りする反応熱を測定する実験を行った。次の文章を読み,下の問い(a・b)に答えよ。H=1.0,N=14,O=16
図1のような発泡ポリスチレンの容器に,水 50.0 g を入れて水温を測定したところ,20.0°C であった。この容器に硝酸アンモニウム 2.00 g を加え,容器を振って水溶液を混ぜながら温度を測定して,図2のグラフを得た。
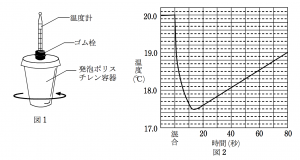
a 硝酸アンモニウムの溶解熱は,いくらになるか。最も適当な数値を,次のうちから一つ選べ。ただし,この水溶液 1 g の温度を 1°C 上昇させるのに必要な熱量は 4.3 J とし,また,溶解熱はすべて水溶液に吸収されたものとする。正解
不正解
-
13問/25問
13. 問題
b 上記の方法によって濃硫酸中の H₂SO₄ の水への溶解熱を求めると,95.3 kJ/mol であった。また,強酸と強塩基の水溶液どうしの中和熱は 56.7 kJ/mol である。1.00 mol/L の水酸化ナトリウム水溶液 1.00 L に,H₂SO₄ 2.00 mol を含む濃硫酸を加えたとき発生する熱量は,いくらになるか。最も適当な数値を,次のうちから一つ選べ。
正解
不正解
-
14問/25問
14. 問題
5.オゾンを含む標準状態の空気 2000 L をヨウ化カリウム水溶液に通じたところ,ヨウ素が生成した。このヨウ素を 0.0100 mol/L のチオ硫酸ナトリウム水溶液で滴定したところ,2.00 mL を要した。ただし,ヨウ素はチオ硫酸ナトリウムと次式のように反応する。
I₂ + 2Na₂S₂O₃ → 2NaI + Na₂S₄O₆
(1) チオ硫酸ナトリウム水溶液による滴定のとき,何を指示薬として加えたらよいか。正解
不正解
-
15問/25問
15. 問題
また、溶液の色が何色から何色になるときを終点とするのか。
- (青, 青紫)色から (無)色
正解
不正解
-
16問/25問
16. 問題
(2) 生成したヨウ素は何 mg か有効数字3桁で答えよ。I=127
- (2.54) mg
正解
不正解
-
17問/25問
17. 問題
(4) 空気 2000 L 中に含まれていたオゾンは何 mol か有効数字3桁で答えよ。
- (1.00)×10⁻⁵ mol
正解
不正解
-
18問/25問
18. 問題
また、体積で何 ppm か有効数字3桁で答えよ。1ppm=10⁻⁶
- (0.112) ppm
正解
不正解
-
19問/25問
19. 問題
6.鉛蓄電池を放電して 5.97×10⁴ C の電気量を取り出した。H=1.0,O=16,S=32,Pb=207,ファラデー定数 9.65×10⁴ C/mol
(1) この放電により,正極の質量は何 g 増加または減少したか有効数字3桁で答えよ。- (19.2)g (増加)
正解
不正解
-
20問/25問
20. 問題
(2) この放電により,硫酸溶液の質量は何 g 増加または減少したか有効数字3桁で答えよ。
- (48.0)g (減少)
正解
不正解
-
21問/25問
21. 問題
(3) 放電前の硫酸溶液の質量が 1000 g,濃度が 32.0 % であったとき,放電後の硫酸の濃度は何 % か有効数字3桁で答えよ。
- (27.4)%
正解
不正解
-
22問/25問
22. 問題
(4) 6.00 A の電流を用いて放電後の鉛蓄電池を放電前の状態に戻すには,何秒間充電しなくてはならないか有効数字3桁で答えよ。
- (9.65)×10³ 秒
正解
不正解
-
23問/25問
23. 問題
7.次の問い (1) ~ (3) に有効数字2桁で答えよ。原子量は H=1.0,C=12,O=16,Na=23,酢酸の電離定数は 2.0×10⁻⁵ mol/L,水のイオン積は 1.0×10⁻¹⁴ mol²/L² とする。また,log2=0.30,log3=0.48 とする。
(1) 0.20 mol/L の酢酸水溶液 の pH はいくらか。正解
不正解
-
24問/25問
24. 問題
(2) 0.20 mol/L の酢酸水溶液 600 mL と 0.20 mol/L の水酸化ナトリウム水溶液 300 mL を混ぜた後,水を加えて全量を 1 L にした。この水溶液の pH はいくらか。
正解
不正解
-
25問/25問
25. 問題
(3) 0.20 mol/L の酢酸ナトリウム水溶液の pH はいくらか。
正解
不正解