第2回Quimica模試【2022年10月30日】
Quiz-summary
0 of 12 questions completed
Questions:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
Information
今から出題される問題に答えよ。(制限時間60分)
You have already completed the quiz before. Hence you can not start it again.
問題を読込中…
You must sign in or sign up to start the quiz.
You have to finish following quiz, to start this quiz:
テスト結果
0問/12問中正解です。
所要時間:
制限時間になりました。
あなたの正解率は0点/0点中0です。
Categories
- Not categorized 0%
-
あなたの偏差値は80です。
-
あなたの偏差値は75です。
-
あなたの偏差値は70です。
-
あなたの偏差値は65です。
-
あなたの偏差値は60です。
-
あなたの偏差値は55です。
-
あなたの偏差値は50です。
-
あなたの偏差値は45です。
-
あなたの偏差値は40です。
-
あなたの偏差値は35です。
-
あなたの偏差値は30です。
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- Answered
- Review
-
1問/12問
1. 問題
正解
不正解
-
2問/12問
2. 問題
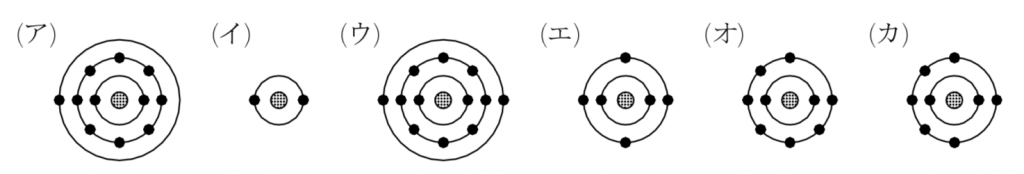
(2) (ア)~(カ)のうち,二価の陽イオンになりやすい原子はどれか。
正解
不正解
-
3問/12問
3. 問題
(3) (ア)~(カ)のうち,単原子イオンになりにくい原子を2つ選べ。
正解
不正解
-
4問/12問
4. 問題
(4) (ア)~(カ)のある原子Xと水素原子からなる多原子イオンには,陽イオンのものや陰イオンのものがある。原子Xは(ア)~(カ)のどれか。
正解
不正解
-
5問/12問
5. 問題
(5) (ア)~(カ)のうち,最外殻電子の数と価電子の数が異なる原子はどれか。
正解
不正解
-
6問/12問
6. 問題
2.水酸化ナトリウム1.00gを水50.0gに溶かした溶液の質量パーセント濃度,モル濃度および質量モル濃度を有効数字3桁で求めよ。ただし,溶液の密度を1.02g/cm³,H=1.00,O=16.0,Na=23.0とする。
- 質量パーセント濃度: (1.96)% モル濃度: (0.500)mol/L 質量モル濃度: (0.500)mol/kg
正解
不正解
-
7問/12問
7. 問題
3.硫酸銅(Ⅱ)水溶液に白金電極を浸し,鉛蓄電池を用いて5.0Aの電流を48分15秒間通じて電気分解した。次の問いに有効数字2桁で答えよ。ただし,原子量はH=1.0,O=16,S=32とし,ファラデー定数F=96500C/molとする。
(1) 鉛蓄電池の負極,正極の質量は,それぞれ何gずつ変化したか。
(2) 電解後の鉛蓄電池の硫酸濃度が25%とすると,電解前の鉛蓄電池の硫酸濃度は何%であったか。ただし,電解後の電解液の質量は100gとする。-
(1) 負極: (7.2)g (増加)(増加または減少) 正極: (4.8)g (増加)(増加または減少) (2) (35)%
正解
不正解
-
-
8問/12問
8. 問題
4.酸素と窒素がそれぞれ21%,79%の体積比で混合した0℃,1.0×10⁵Paの空気がある。0℃,1.0×10⁵Paのもとで1Lの水に酸素は49mL,窒素は23mL溶けるものとして以下の問いに有効数字2桁で答えよ。ただし,N=14,O=16とする。
(1) この空気が飽和している水1Lに溶けている窒素の質量は何mgか。
(2) この空気と接している水2Lに溶けている酸素の体積を標準状態に換算した値は何mLか。-
(1) (23)mg (2) (21)mL
正解
不正解
-
-
9問/12問
9. 問題
(3) 水に溶存している気体を追い出すのに,次のうちで最も効果的なものはどれか。
(ア) 撹拌する (イ) 冷却する (ウ) 加熱して圧力を上げる (エ) 加熱して圧力を下げる (オ) 冷却して圧力を上げる正解
不正解
-
10問/12問
10. 問題
5.SiO₂結晶の生成熱は859kJ/mol,O₂(気)の結合エネルギーは494kJ/molである。ケイ素の単体はダイヤモンドに似た結晶として存在し,結晶中の各Si原子は他の4つの原子と結合している。このSi結晶を壊し,バラバラの原子の状態にするためのエネルギー(格子エネルギー)は368kJ/molである。この場合のSi-Si結合の結合エネルギーは184kJ/molである。以上より,SiO₂結晶におけるSi-O結合の結合エネルギーを有効数字3桁で求めよ。
- (430)kJ/mol
正解
不正解
-
11問/12問
11. 問題
6.次の(a)~(d)の水溶液の25℃におけるpHを,小数第1位まで計算せよ。ただし,アンモニアの電離定数は25℃で2.0×10⁻⁵mol/L,log2=0.30,log3=0.48とする。
(a) 6.0mol/Lの塩酸5.0mLに,水を加えて1.0Lとした。
(b) 0.20mol/Lの水酸化ナトリウム水溶液10mLに,水を加えて1.0Lとした。
(c) 0.20mol/Lのアンモニア水溶液250mLに,水を加えて1.0Lとした。
(d) 0.20mol/Lの塩酸50mLに,0.20mol/Lの塩化アンモニウム水溶液150mLを加えた。- (a) (1.5) (b) (11.3) (c) (11.0) (d) (1.3)
正解
不正解
-
12問/12問
12. 問題
7.水質汚濁の指標の1つである化学的酸素要求量(COD)は,試料水中の有機物を過マンガン酸カリウムなどの酸化剤により酸化分解したときの酸化剤の消費量を求め,それを酸
化剤としてO₂を用いた場合に消費されるO₂の,試料水1Lあたりの質量[mg/L]に換算して表す。いま,有機物のみを含むある試料水のCODを以下の手順で求めた。
[操作1] 試料水100mLをコニカルビーカーにとり,少量の硫酸で酸性にした後,4.00×10⁻³mol/Lの過マンガン酸カリウム水溶液を10.0mL加え,沸騰水浴中で30分間加熱した。
[操作2] 十分量のシュウ酸を混合し,未反応の過マンガン酸イオンの色を完全に消した。
[操作3] 残存しているシュウ酸を, [操作1]と同じ過マンガン酸カリウム水溶液を用いて滴定したところ,終点までに4.52mLを要した。
[操作4] 次に,試料水の代わりに100mLの純水を用いて,上述の[操作1]~[操作3]を同じ条件で繰り返したところ,[操作3]の残存シュウ酸の滴定において0.52mLの過マンガン酸カリウム水溶液を要した。-
次の文章の(1)〜(6)の空欄に適当な数値を入れよ。ただし,O=16とする。
実験操作の結果から, 100mLの試料水中の有機物を酸化するのに要した過マンガン酸カリウム水溶液の体積は(1) (4.00)mL(有効数字3桁)となるので,この体積中の過マンガン酸カリウムの物質量は(2) (1.60)×10⁻⁵mol(有効数字3桁)となる。1molの過マンガン酸カリウムが酸性条件下で酸化剤としてはたらくときには(3) (5)mol(整数値)の電子を受け取る。
一方,O₂が酸化剤としてはたらくときには,1molのO₂は(4) (4)mol(整数値)の電子を受け取る。したがって,100mLの試料水の有機物を酸化するのに要する酸化剤の物質量を,O₂の値に換算すると(5) (2.00)×10⁻⁵mol(有効数字3桁)となるので,この試料水のCODは(6) (6.40)mg/L(有効数字3桁)と算出される。
正解
不正解
-